کلرید قلع (II)، همچنین به عنوان کلرید استنوس شناخته می شود، یک ماده جامد بلوری سفید رنگ می باشد. این ماده یک هیدرات پایدار تشکیل می دهد، اما محلول های آبی آن تمایل به هیدرولیز دارند، به خصوص اگر گرم شوند.
این ماده به طور گسترده ای به عنوان یک عامل کاهنده (در محلول اسید) و در حمام های الکترولیتی برای آبکاری قلع استفاده می شود. لازمه که دقت کنیم و کلرید قلع (II) را با سایر کلریدهای این عنصر مانند کلرید قلع (IV) یا کلرید استانیک (SnCl۴) اشتباه گرفته نشود.خریدوفروش کلرور پالادیوم
دی کلرید قلع در ساختار اتمی خود دارای یک جفت الکترون است، به طوری که مولکول آن در فاز گاز خم می شود. و در حالت جامد، کریستالی زنجیرهایی را به هم متصلی دارد که از طریق پل های کلراید به هم متصل شده اند.
نوع دی هیدرات این ترکیب نیز سه مختصات دارد، که در آن ملکول های آب و قلع پیوند برقرار کرده، و قسمت اصلی ملکول های قلع به صورت دو لایه در شبکه کریستالی قرار می گیرد و آب بین لایه ها جای می گیرد.
خواص و مشخصات شناسایی کلرید قلع (II)
| خواص | مشخصات |
| شکل فیزیکی جامد کریستالی سفید رنگ | فرمول شیمیایی SnCl۲ |
| دانسیته (g/cm۳)۳.۹۵ | وزن مولکولی (g/mol) 189.60 |
| نقطه ذوب (۰C) 247 | شماره (CAS No) ۷۷۷۲-۹۹-۸ |
| نقطه جوش (تخریب ساختار) (۰C) 623 | ساختار کریستالی ساختار لایه ای |
واکنش های شیمیایی
کلرید قلع (II) می تواند در کمتر از جرم خود آب بدون تجزیه آشکار حل شود، اما با رقیق شدن محلول، هیدرولیز ایجاد می شود و یک نمک بازی نامحلول ایجاد می کند:خریدوفروش کلرور پالادیوم
SnCl۲(aq) + H۲O(l) ⇌ Sn(OH)Cl(s) + HCl(aq)
بنابراین، اگر قرار است از محلول های شفاف این ترکیب استفاده شود، لازم است آن را در اسید کلریدریک حل کنید (نوع همان مولار همان یا کلرید استن) و برای حفظ تعادل به سمت چپ (با استفاده از Le Chatelier اصل) پیش رود، محلول های SnCl۲ نیز نسبت به اکسیداسیون هوا ناپایدار هستند:خریدوفروش کلرور پالادیوم
۶SnCl۲(aq) + O۲(g) + 2H۲O(l) → ۲SnCl۴(aq) + 4Sn(OH)Cl (s)
با ذخیره محلول بر روی توده های فلز قلع می توان از این امر جلوگیری کرد.
فرایند کاهش:
موارد زیادی وجود دارد که کلرید قلع (II) به عنوان یک عامل کاهنده عمل می کند، و نمک های نقره و طلا را به فلز و نمک های آهن (III) را به آهن (II) کاهش می دهد، به عنوان مثال:خریدوفروش کلرور پالادیوم
SnCl۲(aq) + 2FeCl۳(aq) → SnCl۴(aq) + 2FeCl۲ (aq)
همچنین مس (II) را به مس (I) کاهش می دهد.محلول های کلرید قلع (II) نیز می توانند به سادگی به عنوان منبع یون های +Sn۲ عمل کنند که از طریق واکنش های بارشی می توانند سایر ترکیبات قلع (II) را ایجاد کنند. به عنوان مثال، واکنش با سولفید سدیم قلع قهوه ای یا سیاه (II) را تولید می کند:خریدوفروش کلرور پالادیوم
SnCl۲(aq) + Na۲S(aq) → SnS(s) + 2NaCl (aq)
اگر ماده قلیایی به محلول SnCl۲ اضافه شود، رسوب سفید اکسید قلع هیدراته (II) در ابتدا تشکیل می شود و سپس در باز اضافی حل می شود و یک نمک استنیت مانند استنیت سدیم تشکیل می دهد:خریدوفروش کلرور پالادیوم
SnCl۲(aq) + 2NaOH(aq) → SnO·H۲O(s) + 2NaCl(aq)
SnO·H۲O (s) + NaOH (aq) → NaSn(OH)۳ (aq)
تولید ترکیبات قلع
از کلرید قلع ۲ خشک می توان در ساخت انواع ترکیبات جالب قلع (II) در حلال های غیرآبی استفاده کرد. به عنوان مثال، نمک لیتیوم ۴-متیل-۲،۶-دی-ترت-بوتیل فنل با SnCl۲ در THF واکنش می دهد و ترکیب دو مختصاته خطی زرد رنگ Sn(OAr)۲ (Ar = آریل) را تشکیل می دهد.خریدوفروش کلرور پالادیوم
کلرید قلع (II) همچنین به عنوان یک اسید لوئیس رفتار می کند، به عنوان مثال کمپلکس هایی با لیگاند مانند یون کلرید تشکیل می دهد:
SnCl۲(aq) + CsCl(aq) → CsSnCl۳(aq)
اکثر این کمپلکس ها هرمی هستند و از آنجا که کمپلکس هایی مانند SnCl۳ دارای هشت ستاره کامل است، تمایل زیادی به افزودن بیش از یک لیگاند وجود ندارد. جفت تنها الکترون در چنین کمپلکس هایی برای اتصال در دسترس است، و بنابراین خود کمپلکس می تواند به عنوان یک پایه یا لیگاند لوئیس عمل کند. این واکنش مربوط به محصول مربوط به فروسن مشاهده شده است:خریدوفروش کلرور پالادیوم
SnCl۲ + Fe(η۵-C۵H۵)(CO)۲HgCl → Fe(η۵-C۵H۵)(CO)۲SnCl۳ + Hg
ترکیبات فلزی:
با استفاده از SnCl2 می توان انواع مختلفی از ترکیبات حاوی پیوندهای فلز – فلز را ایجاد کرد. به عنوان مثال، واکنش با اکتاکاربنیل دی کبالت:
SnCl۲ + Co۲(CO)۸ → (CO)۴Co-(SnCl۲)-Co(CO)۴
نمونه ای از آن می باشد. کلرید قلع (II) بی آب با اثر گاز هیدروژن کلرید خشک روی فلز قلع تهیه می شود و دی هیدرات آن نیز از طریق یک واکنش مشابه و با استفاده از اسید کلریدریک ساخته می شود:
(g)Sn(s) + 2HCl(aq) → SnCl۲(aq) + H۲
سپس آب با دقت از محلول اسیدی تبخیر شده و بلورهای SnCl۲·۲H۲O تولید می کند. این دی هیدرات کردن را می توان با استفاده از انیدرید استیک تا خشک شدن ادامه داد.خریدوفروش کلرور پالادیوم
کاربردهای کلرید قلع (II)
به منظور تهیه قوطی های حلبی، از محلول کلرید قلع (II) حاوی کمی اسید کلریدریک برای آبکاری قلع استفاده می شود، پتانسیل الکتریکی اعمال می شود و فلز قلع از طریق الکترولیز در کاتد تشکیل می شود.خریدوفروش کلرور پالادیوم
کلرید قلع (II) به عنوان ماده ناسازگار در رنگرزی منسوجات استفاده می شود زیرا با برخی از رنگ ها، رنگ های روشن تری به دست می دهد و پوست حلزونی حاصل از این ماده نیز به تنهایی برای افزایش وزن ابریشم استفاده شده است.
در سال های اخیر، تعداد بیشتری از مارک های خمیر دندان مانند g Oral-B یا Elmex کلرید قلع (II) را به عنوان محافظت در برابر فرسایش مینای دندان به فرمول خود اضافه کرده اند. این ماده به عنوان کاتالیزور در تولید اسید پلی لاکتیک پلاستیک (PLA) نیز به کار می رود.خریدوفروش کلرور پالادیوم
کاتالیزور:
این ماده همچنین به عنوان یک کاتالیزور بین استون و پراکسید هیدروژن برای ایجاد فرم تترامریک پراکسید استون کاربرد دارد. کلرید قلع (II) همچنین به عنوان یک عامل کاهنده کاربرد گسترده ای پیدا می کند. این مورد در استفاده از آن برای آینه های نقره ای دیده می شود، جایی که فلز نقره روی شیشه رسوب می کند:خریدوفروش کلرور پالادیوم
Sn۲+(aq) + 2Ag+ → Sn۴+(aq) + 2Ag (s)
کاربرد کلرید قلع (II) در شیمی آلی:
در شیمی آلی، SnCl۲ عمدتا در کاهش استیفن استفاده می شود، به موجب آن نیتریل (از طریق نمک ایمیدوئیل کلرید) به یک ایمین تبدیل می شود که به راحتی به آلدئید هیدرولیز می شود. این واکنش معمولاً با نیتریل های معطر Aryl-CN بهترین عملکرد را دارد. یک واکنش مرتبط (که روش Sonn-Müller نامیده می شود) با یک آمید شروع می شود، که با PCl۵ تصفیه می شود و نمک ایمیدوئیل کلرید تشکیل می شود:خریدوفروش کلرور پالادیوم
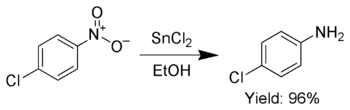
کاهش استیفن امروزه کمتر مورد استفاده قرار می گیرد، زیرا بیشتر با کاهش دی هیدرید دی ایزوبوتیلالومینیم جایگزین شده است. علاوه بر این، کلرید قلع برای کاهش انتخابی گروه های نیترو معطر به آنیلین ها استفاده می شود:خریدوفروش کلرور پالادیوم
کلرید قلع (II) همچنین کینون ها را به هیدروکینون ها کاهش می دهد. کلرید استنوس همچنین به عنوان یک ماده افزودنی غذایی با شماره E512 به برخی از غذاهای کنسرو شده و بطری اضافه می شود، که به عنوان ماده نگهدارنده رنگ و آنتی اکسیدان عمل می کند.